Die wunderbare Welt der Genetik und Molekularbiologie – RNA-Interferenz und Imprinting
BLOG: Bierologie

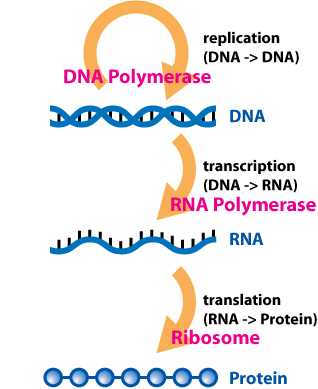
In der Schule wirken Genetik und Molekularbiologie immer so einfach und gut verstanden. Das liegt auch daran, dass man mit den Entdeckungen von Mendel, Watson, Crick und Co nicht nur die Grundlagen sondern auch die Geschichte der Felder nachvollzieht. Die Ergebnisse von Mendel zur Vererbung sind nicht nur aufgrund ihrer relativ einfachen Regeln gut fassbar: Die Einteilung in dominante und rezessive Allele ist gut fassbar, genauso wie die Zahlenverhältnisse der verschiedenen Kreuzungsmodi ihre eigene, simple Schönheit mitbringen. Und auch das zentrale Dogma der Molekularbiologie von Crick, meist über Watsons Beispiel falsch verkürzt zu „von DNA zu RNA zu Protein” wiedergegeben, dürfte noch vielen Menschen im Kopf sitzen.
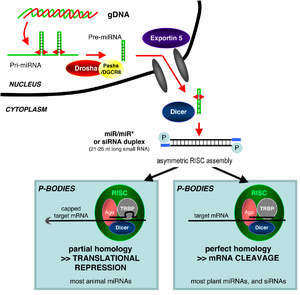
Spannend sind die Ausnahmen solcher vermeintlich allgemein gültigen Regeln. Erst in den 90er Jahren wurde ein Mechanismus namens RNA-Interferenz (RNAi) entdeckt. Dabei werden meist kurze RNA-Stücke aus dem Zellkern herausgeschleust. Diese Stücke binden, in Zusammenspiel mit mehreren Enzymen, an Ziel-RNAs. Diese Ziele werden so davon abgehalten ihre Aufgaben zu erfüllen. Potentielle Ziele sind dabei RNAs von Viren, die so bekämpft werden können, oder auch vom Organismus selbst produzierte mRNAs. In letzterem Fall können Gene über die RNA-Interferenz gesteuert werden. Und bislang gab es hauptsächlich Hinweise dafür, dass diese Beeinflussung der mRNA durch die RNA-Interferenz außerhalb des Zellkerns im Cytoplasma stattfindet.
Eine in PNAS erschienene Veröffentlichung hat sich den Mechanismus am Beispiel der Sojabohne mal etwas genauer angeschaut. In Sojabohnen würde man gerne jene Gene ausschalten oder herunterregulieren die für die Produktion von ungesättigten Fettsäuren verantwortlich sind. Denn ein höherer Anteil an gesättigten Fettsäuren führt zu einer erhöhten Wärmekapazität und die ist gerade bei der Verwendung in der Fritteuse erwünscht. Normalerweise sucht man sich zur RNAi Sequenzstücke auf der fertigen mRNA raus. Allerdings scheint dieser Weg bei der Fettsäure-Produktion, aufgrund von vielen nah-verwandten Genen, nicht ideal, da es schwer ist gezielt einzelne Gene zu treffen.
Deshalb wurden im Versuch mit der Sojabohne Sequenzen aus den Introns, jene Teile die vor der Translation und dem Export der mRNA aus dem Zellkern ins Cytoplasma herausgeschnitten werden (siehe auch meinen Blogpost zu Genomik), ausgewählt. Würde der RNA-Interferenz-Mechanismus nur im Cytoplasma arbeiten dann dürfte man erwarten, dass die intronischen Interferenz-Stücke keine Auswirkungen haben. Allerdings funktioniert das Herunterregeln der Gene trotzdem, wenn auch nicht so effizient wie das bei einer kompletten Ausschaltung der Fall wäre. Sie konnten sogar zerschnittene Prä-mRNA nachweisen, also solche mRNA bei denen die Introns noch nicht entfernt wurden. Die Translation von fertiger mRNA im Cytoplasma wurde durch die Methode übrigens nicht beeinträchtigt.
Damit hat man jetzt erste Anhaltspunkte, dass RNA-Interferenz auch direkt im Zellkern funktionieren kann. Das ist nicht nur ein Nice-To-Know sondern – für Fälle in denen man, aufgrund von zu großer Sequenzähnlichkeit, keine exonischen Ziel-Vektoren für die RNAi hat – eine sehr praktische Sache.
Zumindest die übervereinfachte Variante des molekularbiologischen Dogmas nach Watson stimmt also schon seit längerem nicht mehr. Und auch Mendel hat die Eindeutigkeit schon länger hinter sich gelassen. Der letzte Schrei in Dingen Vererbung dürfte Epigenetik sein: Die Vererbung von unterschiedlichen Phänotypen von der einen Generation zur nächsten, ohne Veränderung der zugrundeliegenden DNA-Sequenz. Meist dadurch hervorgerufen, dass die DNA an den entsprechenden Stellen so modifiziert wird, dass eine Transkription nicht mehr möglich ist.
Bislang scheint es so zu sein, dass die meisten beobachteten Anpassungen zwar keine permanenten Änderungen hervorrufen und im Laufe einiger Generationen wieder verschwinden, aber das ist, zumindest evolutionär gesehen, auch gar nicht notwendig. Eine “schnelle”, temporäre Anpassung, von der einen Generation zur nächsten kann ein evolutionärer Fitness-Vorteil sein, da man seine Nachkommen z.B. auf die Umweltbedingungen primen kann.
Eine besonders spannende Form von Epigenetik ist das „Genomic Imprinting”. Bei Genen die davon betroffen sind hängt die Aktivität davon ab, von welchem Elternteil man die Kopie des Gens bekommen hat. Und auch bei dieser Form werden Gene über chemische Modifikationen an der DNA selbst oder an Modifikationen DNA-bindenden Proteinen. Die momentan am vielversprechendsten klingende Theorie zum Ursprung des Mechanismus heisst „Kinship Theory” und bezieht sich, wie so oft in der Biologie, auf Fitness-Vorteile. Denn bei Arten die sich geschlechtlich fortpflanzen kann man nicht nur die direkte Fitness (Wie gut gebe ich meine Gene durch meine Nachkommen an die nächste Generation weiter) sondern auch die indirekte Fitness (Wie geben Nahverwandte, wie Geschwister, meine Gene weiter).
Wenn man die Gesamtfitness (direkt + indirekt) betrachtet ergeben sich für Mutter und Vater zwingend andere Zielsetzungen bei der Nachkommenproduktion. Väter haben keinen indirekten evolutionären Vorteil davon, wenn die Mutter weitere Nachkommen zeugt (außer sie sind wieder der Vater). Mütter (bzw. ihre Gene), auf der anderen Seite, müssen hingegen abwägen wie viel Energie sie in einzelne Nachkommen stecken: Ab einem gewissen Schwellenwert ist es sinnvoller nicht mehr Energie in einzelne Nachkommen zu stecken sondern lieber mehr davon zu produzieren.
Und genauso verhalten sich Gene die dem Imprinting unterliegen auch: Gene die dafür sorgen, dass Mütter vor oder kurz nach der Geburt viel Energie in ihre Nachkommen stecken müssen, sind ausgeschaltet wenn sie von der Mutter vererbt werden und aktiv wenn sie vom Vater vererbt werden. Genau umgekehrt verhält es sich bei Genen die dafür sorgen, dass Mütter weniger Energie in die Nachkommen stecken: Sie sind bei Vererbung durch die Mutter aktiv, bei der Vererbung durch den Vater inaktiv. Aber wie kommt es zu diesem „alles oder nichts” bei der Gen-Aktivität? Das Konzept nennt sich „The Loudest Voice Prevails” und wird von Jon Wilkens (dessen Blog ich zu dem Thema nur empfehlen kann) sehr schön mit einer Analogie erklärt:
Stellen wir uns vor 2 kommunikationsverarmte Soziopathen, Alice und Bob, sitzen zusammen in einem Büro und möchten die Temperatur regeln. Alice mag die Raumtemperatur bei 20 °C, Bob bei 21 °C. Beide haben als einzige Option jeweils einen kleinen Heizlüfter um die Temperatur zu steuern. Alice kann die Leistung ihres Lüfters etwas herunter regeln um auf die 20 °C zu kommen. Bob kann dafür im Gegenzug seinen Lüfter etwas weiter hoch regeln um wieder auf die 21 °C zu kommen. Und so spielen beide an den Reglern. Allerdings funktioniert das Prinzip nur so lange bis Alice ihren Heizlüfter komplett ausgeschaltet hat, Bob hingegen kann an dem Punkt seinen Regler noch weiter hochdrehen und hat am Ende bei 21 °C „gewonnen”. Hätten beide anstelle eines Heizlüfters eine Klimaanlage würde Alice gewinnen, denn Bob muss seine irgendwann komplett abschalten um es noch wärmer zu kriegen, während Alice noch weiter herunter regulieren kann.
Und vergleichbar funktioniert es auch bei der Vererbung mit Imprinting: Bei Genen die viel Energie von der Mutter einfordern läuft so ein Regelkreis (in evolutionärer Zeit) so lange ab bis man auf das beobachtete Muster (vererbt von Mutter = aus, vererbt von Vater = aus) findet. Und halt andersrum für die Gene die dafür sorgen, dass Mütter weniger Energie pro Nachkommen investieren.
Es ist doch schön zu sehen, dass die Biologie neben den weitbekannten Mechanismen noch ein paar Überraschungen bereit hält. Und ich bin gespannt welcher Mechanismus als Nächstes alte Dogmen über den Haufen werfen wird.
Grafik zentrales Dogma Wikimedia, CC-BY-SA 3.0
Grafik RNAi Wikimedia CC-BY 2.0
Foto Passive-aggressive Wilbanks, CC-BY-SA 2.0
Hoffer, P., Ivashuta, S., Pontes, O., Vitins, A., Pikaard, C., Mroczka, A., Wagner, N., & Voelker, T. (2010). Posttranscriptional gene silencing in nuclei Proceedings of the National Academy of Sciences, 108 (1), 409-414 DOI: 10.1073/pnas.1009805108
Haig, D. (2000). THE KINSHIP THEORY OF GENOMIC IMPRINTING Annual Review of Ecology and Systematics, 31 (1), 9-32 DOI: 10.1146/annurev.ecolsys.31.1.9





Um bei der Geschichte zu bleiben, dass nicht alles so simpel ist wie im Lehrbuch: Ich hab zuerst gedacht, dass die nur unter der Annahme gearbeitet haben, splicing könnte ausschließlich im Nucleus stattfinden, also muss RNAi an Introns im Kern passieren. Das muss so nicht unbedingt stimmen, weil zumindest das alternative “minor spliceosome” wohl (auch) im Cytoplasma arbeitet.
Hab dann aber mal nen kurzen Blick in das PNAS Paper geworfen, die haben ja fein wie es sich gehört den Nucleus fraktioniert, die RNAs scheinen also wirklich schon innerhalb des Kerns geschnitten zu werden. Das Problem ist nur: die haben mit Pflanzen gearbeitet, und RNAi unterscheidet sich wohl in vielen Punkten in Tieren und Pflanzen. Es ist beispielsweise gar nicht überraschend, dass es keine translational repression gab. Die ist in Pflanzen sowieso extrem selten.
Allerdings ist das Paper ein kleiner Schritt in der Erklärung einer damals komischen Beobachtung: Vor zehn Jahren haben Leute vom australischen CSIRO verschiedene dsRNA-Konstrukte auf ihre RNAi-Wirksamkeit verglichen. Dabei war dann eine Haarnadelstruktur effektiver als ein simples lineares dsRNA Molekül. Aber jetzt kommt das komische, wenn im loop des Haarnadelmoleküls ein Intron drin war, war die RNAi noch effektiver. Möglicherweise, und das stützt das aktuelle PNAS-Paper, arbeiten die Proteine für RNAi und Spliceosome zusammen. Spannend!
Fitness und Energie
Interessant, was Du in dem Artikel zu Fitness und Energie auf Ebene der Gene schreibst. Das passt gut zu meinem Artikel der das gleiche Thema auf der Ebene der Organismen behandelt.
Hast Du Dir mal die Methylierungskarte des menschlichen Genoms angesehen?