Als sich die Amphibien auf die Beine machten
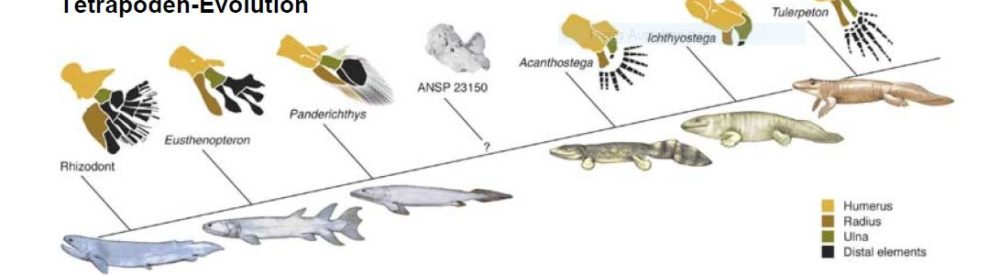
Evo-Devo rockt! Evo-Devo ist ein aus den USA stammender Jargon für die Forschung an der Schnittstelle von Ontogenese und Phylogenese, also der Biologie der Individualentwicklung und der Evolutionsbiologie. Evo-Devo steht dabei als Kurzwort für „evolutionary developmental biology“, die evolutionäre Entwicklungsbiologie. Vor einiger Zeit publizierten in diesem Fachgebiet Paläontologen des Museums für Naturkunde Berlin und des Leibniz-Instituts für Evolutions- und Biodiversitätsforschung einen sehr interessanten Artikel über Amphibien in Nature [1].
Amphibien stammen von frühen Quastenflossern ab und entwickelten sich vor 360 Millionen Jahren. Sie waren die ersten Wirbeltiere, die an Land gingen und entwickelten im Laufe der Zeit aus muskulären, gelenkig gegliederten Flossen vier Laufbeine.
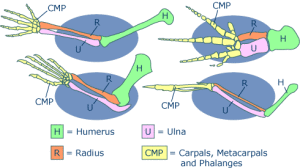
Diese Laufbeine begründen den Oberbegriff Tetrapoden (Vierbeiner) für die landlebenden Wirbeltierklassen Amphibien, Reptilien, Vögel und Säugetiere. Auch wenn sich bei manchen Tetrapoden die Vorderbeine zu Armen und Flügeln umwandelten, ist der grundlegende Knochenbau dieser Gliedmaßen im Laufe der Evolution gleich geblieben.
Heute gibt es drei Ordnungen von Amphibien: Frösche und Kröten (Anura; Froschlurche); Salamander und Molche (Caudata; Schwanzlurche) und Blindwühlen (Gymnophiona), die von einem gemeinsamen Vorfahren abstammen. Fast alle Amphibien machen im Laufe ihres Lebens eine sogenannte Metamorphose durch, was bedeutet, dass sich ihre Gestalt verändert. Einfaches Beispiel dafür ist der Frosch. Aus dem befruchteten Laich entwickelt sich zunächst die Larve, die sogenannte Kaulquappe. Diese wächst mit den Wochen und verwandelt sich in mehreren Schritten zu einem Frosch, dabei entwickeln sich auch die Beine. Mit Abschluss der Metamorphose ist aus der einstigen Larve ein erwachsenes Tier geworden. Die meisten Amphibien wechseln mit der abgeschlossenen Metamorphose auch den Lebensraum. Kaulquappen sind reine Wasserbewohner mit Kiemenatmung. Frösche atmen über ihre Lungen, die sich während der Metamorphose entwickeln.
Die Regeneration der Beine bei den Molchen
Unter den Wirbeltieren weisen die Salamander und Molche bei Weitem die größten Regenerationsfähigkeiten auf. Einige Biologen untersuchten dabei besonders die Regeneration der Beine bei den Molchen. G. Wolff (1910) wies die Abhängigkeit der Extremitätenregeneration von der Nervenversorgung nach. Forscher vermuteten, dass die Nervenendigungen (Synapsen) einen Mitose stimulierenden Faktor freisetzen. A.L. Mescher und D. Godspodarowicz (1979) isolierten eine solche Substanz, den Fibroblast Growth Factor. In einem eleganten Experiment mit Molchlarven konnte Günther Hertwig (1927) zeigen, dass das Material, aus dem sich das Beinregenerat aufbaut, aus der unmittelbaren Nachbarschaft der Amputationswunde stammen muss. Er transplantierte Beine einer haploiden Larve auf Beinstümpfe einer diploiden. Nach dem Anheilen amputierte er das Transplantat bis auf eine schmale Scheibe. Das Regenerat wies anschließend – mit Ausnahme eingewanderter Blutgefäßzellen – nur haploide Zellen auf. B. M. Carlson (1972) zeigte, dass das Beinregenerat eine normal entwickelte Muskulatur aufwies, wenn zuvor 99 % der Muskelzellen aus dem Amputationsstumpf entfernt worden waren. Es müssen also Nicht-Muskelzellen in der Lage sein, Muskulatur im Regenerat zu bilden. Borivoje Dim. Milojević (1924) transplantierte Regenerationsblasteme des Vorderbeins eines Molchs (Gattung Triturus) auf frisch amputierte Hinterbeine und umgekehrt. Waren die Transplantate jünger als 12 Tage, differenzierten sie sich ortsgemäß, waren sie älter, differenzierten sie sich herkunftsgemäß. Paul Weiss (1926) zeigte schließlich, dass auf einem längs halbierten Extremitätenstumpf ein vollständiges Regenerat entsteht. Die Regenerationsknospe zeigte also – so Paul Weiss – Eigenschaften eines „harmonisch-äquipotentiellen Systems“.
Woher “weiß” der gerade nachwachsende Abschnitt eines Glieds, wie viel von dem Ganzen verloren gegangen und nun zu ersetzen ist? Warum bildet die Haut keine Narbe, die den Stumpf definitiv versiegelt? Anscheinend handelt es sich bei der Regeneration eines Beins praktisch um die Rekapitulation eines larvalen Prozesses. Demnach sollte beiden Vorgängen das gleiche genetische Programm zugrunde liegen. Wie kann ein Molch so spät noch auf dieses larvale Programm zurückgreifen, um ein Bein immer wieder von Grund auf neu entstehen zu lassen? Wird dieses larvale Programm durch Hox-Gene gesteuert? Hox-Gene steuern die Verteilung bestimmter Zellgruppen in einem bestimmten Areal des Körpers während der Embryonalentwicklung und sind als Hauptschalter für die Realisierung der Baupläne aller Tiere zuständig. Die Besonderheit der Hox-Gene ist die Tatsache, dass von ihnen mehrere andere, funktionell zusammenhängende Gene im Verlauf der Embryonalentwicklung bzw. Morphogenese gesteuert werden. Man kann Hox-Gene als übergeordnete genetische Informationsstruktur ansehen, da sie die Entwicklung nicht direkt, sondern durch Regulation anderer Gene steuern. Mutationen in Hox-Genen sind meist tödlich oder haben gravierende Auswirkungen auf die Entwicklung.
HOX Genes and Limb Evolution
Für die kambrische Artenexplosion war nach Stephen Jay Gould die Evolution der Hox-Gene zumindest mitverantwortlich. Dies wäre eine mögliche Erklärung für die rasche Entwicklung neuer Arten in einer kurzen Epoche. Nach der Hox-Gen-These könnte sich in einem primitiven Wesen mit einem Ur-Hox-Gen, das sich zufällig einmal verdoppelt, ein Organismus mit neu erworbenen Eigenschaften entwickeln. Ein Indiz, das diese These unterstützt, ist die Polydaktylie. Menschen mit Polydaktylie verfügen über mehr als die übliche Anzahl an Fingern oder Zehen. Besonders häufig findet sich ein- oder beidseitig ein jeweils sechster Finger (meist ein Doppeldaumen) oder Zeh (Hexadaktylie). Da polydaktyle Finger oder Zehen kein homologes Merkmal besitzen, das heißt, da an der Stelle eines neuen Fingers beim Wildtyp weder Zellen noch Gewebe existieren, kann ein polydaktyler Finger oder Zeh – evolutionsbiologisch gesehen – auch als eine komplette phänotypische Innovation betrachtet werden.
Salamander haben ein ungewöhnlich hohes Regenerationsvermögen und können wiederholt und während ihres ganzen Lebens durch Amputationen oder Verletzungen verlorene Beine und Schwänze vollständig regenerieren. Bei Kröten und Fröschen – gelingt dies nur als Kaulquappe also im Larvenstadium.
Die Regeneration des Beines nach Amputation beim Salamander
Generell unterscheiden sich allerdings Salamander nicht nur in dem Regenerationsvermögen ihrer Beine von anderen Landwirbeltieren, sondern auch darin, wie sich ihre Beine zu Beginn bilden. Salamander bilden ihre Finger in der umgekehrten Reihenfolge wie alle anderen Tetrapoden, ein Phänomen, was Biologen schon seit über hundert Jahren Rätsel aufgibt. Die Frage, die sich nun stellte, war, ob dieser andersartige Weg der Beinentwicklung und das hohe Regenerationsvermögen evolutiv miteinander zusammenhängen.
Beinentwicklung und Schwanzregeneration bei den Tetrapoden des Oberen Karbon und Unteren Perm
Eine Arbeit von Nadia B. Fröbisch, Constanze Bickelmann, Jennifer C. Olori und Florian Witzmann gab die Antwort: Nein. Sie widerlegten diesen Zusammenhang in einer Studie an verschiedenen Fossilien von Tetrapoden, die vor 300 Millionen Jahren lebten [1]. Die Fossilien stammen aus Sammlungen verschiedener Naturkundemuseen und fossilisierten unter sehr guten Erhaltungsbedingungen. Zusätzlich enthielten diese Sammlungen eine große Anzahl von Individuen aus verschiedenen Entwicklungsstadien.
Die Wissenschaftler verglichen bei Sclerocephalus, Apateon, Micromelerpeton, Microbrachis und Hyloplesion die Reihenfolge der Verknöcherung der Gliedmaßen in verschiedenen Larvenstadien und konnten so Rückschlüsse auf die damalige Beinentwicklung ziehen. In Fossilmaterial von Microbrachis und Hyloplesion fanden sie starke Hinweise auf die Regenerierung der knöchernen Schwanzwirbel, die begleitet wurde von einer Differenzierung der Zellen in der Nachbarschaft dieser Wirbel. Sie folgerten daraus, dass Microbrachis und Hyloplesion in der Lage waren ihren Schwanz zu regenerieren.
Die Forscher zeigten, dass in den Erdzeitaltern des Oberen Karbon und Unteren Perm verschiedene Gruppen von Tetrapoden in der Lage waren, ihre Beine wie der heutige Salamander zu regenerieren. Sie konnten diese Regenerationsfähigkeit sowohl bei fossilen Gruppen nachweisen, die ihre Beine wie die Mehrheit der heute lebenden Tetrapoden entwickeln, als auch bei solchen, die ein umgekehrtes Muster der Beinentwicklung wie beim heutigen Salamander aufweisen. Die hohe Regenerationsfähigkeit ist also vermutlich eine ursprüngliche Fähigkeit, die im Laufe der Evolution der verschiedenen Tetrapoden mindestens einmal, möglicherweise aber auch mehrfach unabhängig voneinander verloren ging, darunter auch in der Linie zu den Säugetieren.

Heute ist der Querzahnmolch Axolotl (Ambystoma mexicanum) der Weltmeister der Bein-Regeneration. Ich vermute, dass die Ursache für seine sehr hohe Regenerationsfähigkeit seine Neotenie ist. Neotenie bezeichnet in der Zoologie den Eintritt der Geschlechtsreife im Larvenzustand ohne Metamorphose. Axolotl verbleibt zeitlebens im kiemenatmenden Larvenstadium und lebt daher nur im Wasser. Zusätzlich ist er in der Lage sich zu fortzupflanzen. Diese Neotenie wird durch eine angeborene Unterfunktion der Schilddrüse verursacht, d.h. sie produziert nicht genügend für die Metamorphose notwendige Hormone (Thyroxin, Trijodthyronin oder Thyroidea) bzw. das normal hervorgebrachte Hormon wird nicht in die Blutbahn ausgeschüttet.
Ein Molchmodell für Sympodie
Als Anhänger der evolutionären Medizin hoffe ich, dass die Arbeiten von Fröbisch et al. und anderen Wissenschaftlern eines Tages helfen werden ein Molchmodell für Sympodie zu entwickeln. Sympodie oder Meerjungfrauensyndrom ist eine sehr seltene Entwicklungsstörung beim Menschen, bei der die Beine ab dem Becken abwärts zusammengewachsen sind. Der Pathologe August Förster hat 1865 drei Varianten unterschiedlichen Schweregrads beschrieben. In leichteren Fällen sind die Beine zwar angelegt, aber miteinander verschmolzen; in schweren Fällen sind die Unterschenkel – oder die gesamten Beine – nur rudimentär vorhanden. Fast immer bestehen gleichzeitig weitere Fehlbildungen der Arme und der inneren Organe, wie das Fehlen der Niere auf einer Seite oder beiden Seiten. Die Kinder sind daher selten lebensfähig. 70 % der Feten werden tot geboren, die übrigen sterben kurz nach der Geburt.
Die Regeneration der Beine bei den Molchen ist ein gut untersuchtes Modellsystem, das bereits seit mehr als 90 Jahren erforscht wird. Eine freischwimmende Larve, die ihre Beine entwickelt lässt sich leichter beobachten als z. B. ein Mausfötus im Mutterleib. Die Larven sind klein und lassen sich in großer Anzahl halten. Axolotl hat zusätzlich den Vorteil, das es sein ganzes Leben im Larvenstadium verbringt. Leider ist das Axolotlgenom zehn Mal größer als das menschliche Genom und noch nicht sequenziert. Eine Arbeitsgruppe hat aber bereits mit dem CRISPR-Cas9-System zielgerichtete Mutationen in das Axolotlgenom eingeführt [2]. Einiges ist also bereits geschafft auf dem Weg zu einem Molchmodell aber es liegt vor allem auf der genetischen Seite noch viel Arbeit vor uns.
Weiterführende Literatur
Schlangen-DNA macht Mäuse beinlos
[1] Nadia B. Fröbisch, Constanze Bickelmann, Jennifer C. Olori & Florian Witzmann (2015) Deep-time evolution of regeneration and preaxial polarity in tetrapod limb development Nature 527, 231–234.
Bildnachweis
Abb.2: Aufbau der Knochen des Vorderbeins bzw. Arms, Flügels, Flosse bei Wirbeltieren
Image credit: This image was created by the University of California Museum of Paleontology’s Understanding Evolution (http://evolution.berkeley.edu).
Abb.3: Querzahnmolch Axolotl (Ambystoma mexicanum)
Autor: Faldrian
Datum: 5 Juni 2013
Titel: Axolotl in der biologischen Lehrsammlung der de:Universität Konstanz.
Quelle: https://commons.wikimedia.org/wiki/File:Axolotl_Uni_Konstanz.JPG
Lizenz: This file is licensed under the Creative Commons Attribution-Share Alike 3.0 Unported license.


Pingback:[SciLogs] Als sich die Amphibien auf die Beine machten
Gliedmassenregeneration wäre auch für Amputierte besser als jede Prothese. Mindestens heute, wo Prothesen keine Gefühlssensationen vermitteln. Ausgeschlossen ist eine Regeneration von Gliedmassen beim Menschen nicht – auch wenn die Regeneration bereits seit 90 Jahren an Molchen erforscht wird und trotzdem keine Erkenntnisse für den Menschen abgefallen sind. Mindestens die Fingerkuppe kann sogar der Mensch regenerieren, auch wenn diese Methode nicht allen bekannt ist.
In der Biologie und Medizin gibt es viele Gebiete, die schon viele Jahrzehnte erforscht werden und wo es bis jetzt keinen Durchbruch gab. Doch das schliesst zukünftige Durchbrüche nicht aus wie beispielsweise die Krebsimmuntherapie zeigt, welche bereits viele Jahrzehnte erforscht wird oder in die mindestens seit vielen Jahrzehnten Hoffnungen gesetzt wurde, die aber erst jetzt Eingang in den klinischen Alltag gefunden hat.
Schöner Artikel! Wie werden eigentlich die Anzahl der Finger und Gliedmaßen festgelegt? Hängt das auch mit den Hox-Genen zusammen?
Die Hox-Gene findet man zuerst bei Cnidariern, richtig? Wie kann man sich vorstellen, wirkt sich die Verdoppelung eines Hox-Gens aus? Entsteht dann ein neuer Körperabschnitt? Oder ein neues Gliedmaß (bzw. Tentakel oder so?)?
Danke! Freut mich, dass Dir der Artikel gefallen hat. Bei der Festlegung der Anzahl der Finger und Gliedmaßen spielen die Hox-Gene auch eine wichtige Rolle. Schau Dir mal dieses Paper an: Why we have (only) five fingers per hand: Hox genes and the evolution of paired limbs
Hox-Gene sind bisher nur bei Vielzellern entdeckt worden und Cnidarier scheinen die ersten gewesen zu sein. Sie haben zwei Hox-Gene. Schwämme und Rippenquallen haben keine Hox-Gene. Tetrapoden besitzen 39 Hox-Gene, die sich in vier Gencluster einteilen lassen. Es wird angenommen, dass sich Hox-Gene im Verlaufe der Evolution der Wirbeltiere zweimal komplett verdoppelt haben. Ich denke eine Verdopplung eines Hox-Gens alleine wird erstmal nicht zu einer Entstehung eines neuen Körperabschnitts oder Gliedmaß führen. Da müssen bestimmt noch einige Dinge hinzu kommen: Eine neue Regulation der Genexpression und Mutationen in dem neuen Hox-Gen, die zu einer Änderung der Sequenzspezifität des Proteins (Transkriptionsfaktor) führen. Polydaktylie wird autosomal dominant vererbt, wenn es ein alleiniges Merkmal ist. Wenn es mit anderen Symptomen Teil eines Syndroms ist, wird es autosomal rezessiv vererbt.